5月13日,Signal Transduction and Targeted Therapy期刊在线发表了以我校为第一单位、题为“Enhanced potency of an IgM-like nanobody targeting conserved epitope in SARS-CoV-2 spike N-terminal domain”的研究论文(SCI一区Top,影响因子39.3)。我校与中科院微生物研究所联合培养2020级博士研究生刘博,中国科学院微生物研究所博士后刘红辉和韩普、中国科学院微生物研究所博士生王晓云为该论文的共同第一作者。我校动物医学学院微生物学与免疫学创新研究导学团队博士生导师王奇慧研究员,山西省“131”工程领军人才、特聘教授、博士生导师高福院士,导学团队负责人、博士生导师田文霞教授及中国疾病预防控制中心武桂珍研究员为该论文的共同通讯作者。
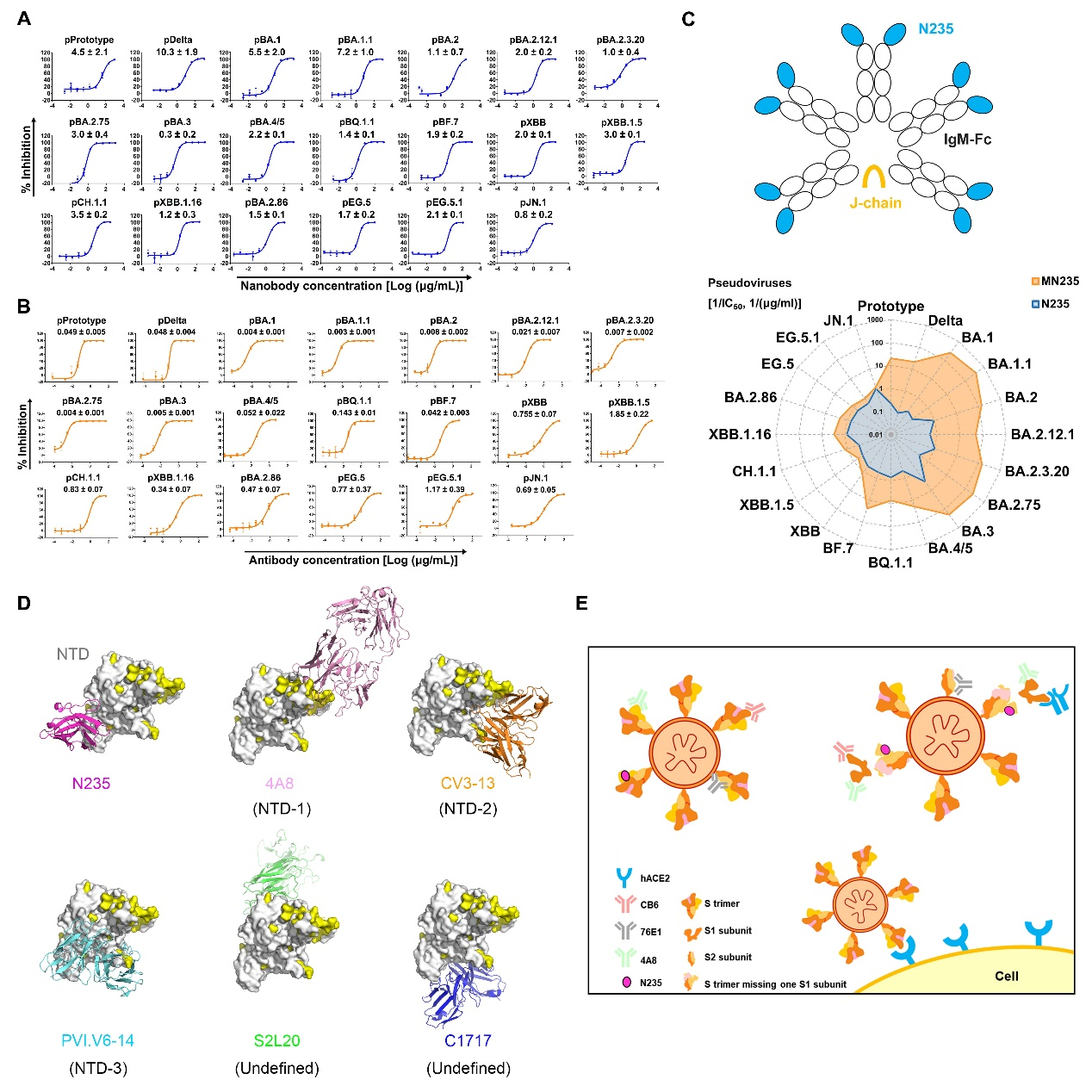
新冠病毒Omicron亚型突变株持续在全球流行,威胁着人类公共卫生安全。已有研究报道了靶向NTD的抗体可能通过调节S的构象变化或与细胞表面的糖结合参与病毒的入侵和感染,因此NTD也可以作为重要靶点来诱导产生特异性的抗体。研究团队筛选到一株广谱纳米抗体N235,对SARS-CoV-2原型毒株和Omicron系列亚型突变株(包括近期出现的亚型突变株XBB、EG.5和JN.1等)均表现出良好的亲和力和中和效果,且结合常数与中和活性呈现一定的正相关性:结合力越强,其中和活性越高。结构生物学研究发现,N235识别NTD上一个新的、保守的表位:位于整个S三聚体的内部,并于邻近S上的RBD有明显的空间位阻,推测其通过破坏S三聚体的稳定性或诱导S1亚基脱落来发挥中和作用。进一步通过流式结合试验、Western-blot等试验验证了该假设,结果表明N235可能通过破坏S三聚体的稳定性并诱导S1亚基脱落来发挥抗病毒效果(如下图所示)。此外,研究团队将纳米抗体N235与人IgM Fc区融合,构建获得十价IgM型抗体MN235。与单价N235相比,MN235在体外假病毒中和活性上表现出不同程度的增强,且进一步研究表明该IgM型抗体能通过诱导S1脱落和交联病毒颗粒的双重机制发挥抗病毒作用。在小鼠模型上,低剂量鼻内给药MN235可有效预防Omicron亚型突变株BA.1和XBB假病毒的感染,提示其可作为一种有前景的候选抗体。
该研究获得了国家重点研发计划、国家杰出青年科学基金和中国科学院稳定支持基础研究领域青年团队项目的支持。
近几年来,我校外聘博士生导师高福院士团队与我校田文霞教授团队共同为我校培养20余名研究生,目前已毕业6名博士、7名硕士;其中牛胜博士论文获山西省优秀博士论文,刘博博士论文本年度推荐为山西省优秀博士论文;毕业研究生以第一或共同第一作者在Cell、TheEMBO Journal、Proc Natl Acad Sci U S A、ScienceBulletin、Cell Reports、Signal Transduction and Targeted Therapy、National Science Review、Cell Reports Medicine、JournalVirology等国际高水平期刊发表论文10余篇,其中2篇为封面论文。
论文链接:https://doi.org/10.1038/s41392-024-01847-8